Ophtalmologie
Publié le 15 oct 2017Lecture 16 min
Œdème maculaire diabétique - Comment optimiser sa prise en charge ?
Sylvie FELDMAN-BILLARD, Service de médecine interne, Centre hospitalier national d’ophtalmologie des Quinze-Vingts, Paris

Principale cause de malvoyance chez les patients diabétiques, l’œdème maculaire diabétique (OMD) est défini par un épaississement au niveau de la macula lié à une accumulation de liquide dans la rétine(1). Sa prévalence globale est estimée à 7 % d’après les dernières données des études internationales(2). Elle varie selon la durée du diabète ainsi que le niveau de contrôle glycémique ou tensionnel. Bien qu’elle soit en diminution ces dernières années, probablement en raison d’une optimisation de la prise en charge du diabète et de la pression artérielle, sa fréquence reste préoccupante. En effet, l’OMD concerne aujourd’hui près d’un patient diabétique sur 15 et plus de 20 millions de personnes dans le monde(2).
La prise en charge de l’OMD a considérablement évolué ces dernières années depuis l’avènement des nouvelles techniques d’imagerie et de traitement(1). La tomographie en cohérence optique (OCT) permet de détecter l’OMD à un stade très précoce, d’en suivre l’évolution et de guider le traitement. Les injections par voie intravitréenne (IVT) d’antiangiogéniques ou de corticoïdes ont aussi largement contribué à améliorer le pronostic oculaire des patients atteints d’OMD. Mais, en aucun cas, ils ne permettent de s’affranchir du contrôle optimal des facteurs systémiques (glycémie et pression artérielle), pierre angulaire du traitement.
Mécanismes intervenant dans la pathogénie de l’OMD
(figure 1)
Figure 1. Physiopathogénie de l’œdème maculaire diabétique. IL-6 : interleukine 6, TNFα : tumor necrosis factor-α, ICAM1 : intercellular adhesion molecule, MCP-1 : monocyte chemoattractant protein-1, MMP : matrix metalloproteinase, Ang-2 : angiopoïétine 2
La pathogénie de l’OMD est complexe et fait intervenir de nombreux mécanismes(3). Si elle n’est encore que partiellement élucidée, sa meilleure compréhension a déjà contribué au développement des nouvelles approches thérapeutiques.
L’hyperglycémie chronique est l’élément principal impliqué dans la pathogénie de l’OMD. Par le biais de l’activation des quatre voies biochimiques (polyols, produits avancés de la glycation, protéine kinase C et hexosamines), elle augmente le stress oxydatif, l’inflammation, l’hypoxie et la dysfonction vasculaire. En résulte une augmentation de production de facteurs de croissance, dont le vascular endothelial growth factor (VEGF), mais aussi de cytokines. Toute cette cascade d’événements est à l’origine de lésions tissulaires conduisant à une hyperperméabilité et à une fuite vasculaire. La rupture de la barrière hémato-rétinienne interne, principal mécanisme à l’origine de l’OMD, est liée à l’altération des systèmes de jonction situés entre les cellules endothéliales rétiniennes.
En outre, tout facteur induisant une augmentation de la pression hydrostatique (hypertension artérielle, insuffisance cardiaque ou rénale) ou une diminution de la pression oncotique (hypo-albuminémie) peut aggraver l’OMD. Ils doivent être recherchés et traités le cas échéant.
Éléments diagnostiques de l’OMD
(figure 2)
Figure 2. Éléments diagnostiques de l’OMD.
Baisse de l’acuité visuelle
La baisse d’acuité visuelle (AV), variable d’un patient à l’autre, est en général lente et progressive. Lorsque l’épaississement atteint la fovéa, le patient devient symptomatique.
Examen biomicroscopique et photographie du fond d’œil
Le diagnostic clinique de l’OMD repose sur la présence d’un épaississement rétinien ou d’exsudats lipidiques dans la région maculaire. L’atteinte peut être localisée ou diffuse. Si des logettes intra-rétiniennes maculaires sont visualisées, elles définissent l’œdème maculaire cystoïde. Les photographies du fond d’œil évaluent également la sévérité de la rétinopathie diabétique (RD) associée.
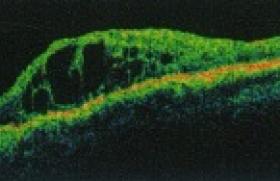
Tomographie en cohérence optique (OCT)
L’OCT joue un rôle central dans la prise en charge de l’OMD. Outre le diagnostic, il permet de quantifier l’œdème, d’en définir la localisation en analysant la cartographie rétinienne et de suivre son évolution de manière précise et reproductible.
Angiographie à la fluorescéine
L’angiographie à la fluorescéine participe au bilan de l’OMD. Elle permet de localiser l’origine des diffusions à partir de microanévrysmes et de détecter des zones de non-perfusion ou une ischémie maculaire. Cet examen pourrait être prochainement supplanté par une nouvelle technique d’imagerie non invasive, l’OCT-angiographie, qui offre une analyse tridimensionnelle de la vascularisation maculaire sans injection de colorant.
Classification de l’OMD
(tableau)
La classification actuelle de l’OMD, détaillée dans le tableau, permet d’établir des stades de gravité assortis de pronostic visuel spécifique. Évaluée à partir de photographies, elle est fondée sur la localisation de l’OMD par rapport au centre de la macula. Plus l’œdème est proche du centre, plus la menace visuelle est grande. Un épaississement maculaire proche de la fovéa définit l’OMD cliniquement significatif. Exposant à un risque élevé de baisse visuelle, il justifie d’envisager un traitement. Par ailleurs, certains éléments associés tels qu’une ischémie maculaire sont de mauvais pronostic.
Cette classification, fondée actuellement sur l’analyse de photographies, évoluera certainement lorsque la valeur pronostique des signes observés en OCT sera établie. En outre, si les prochaines études épidémiologiques établissent le diagnostic d’OMD à partir des données d’OCT, l’estimation des taux de prévalence sera probablement revue à la hausse.
Facteurs de risque de l’OMD
(figure 3)
Figure 3. Facteurs de risque ou d’aggravation de l’OMD. En rouge : facteurs de risque majeurs En noir : facteurs de risque au rôle plus modeste ou discuté.
Les facteurs de risque majeurs de l’OMD sont la durée d’évolution du diabète, l’hyperglycémie chronique, l’hypertension artérielle et la sévérité de la RD. Ainsi, le risque d’OMD est multiplié par 4 après 20 ans d’évolution du diabète, comparé à des patients ayant moins de 10 ans de durée d’évolution ou chez les patients dont les taux d’HbA1c sont supérieurs à 9 % vs 7 %(2). Il est, en outre, double chez les patients hypertendus(2). D’autres facteurs de risque sont discutés et leur rôle est probablement plus modeste :
– la dyslipidémie est associée à une augmentation modérée du risque d’OMD ;
– la néphropathie et/ou la protéinurie, en induisant une diminution de la pression oncotique et une augmentation de la surcharge volémique, apparaissent comme facteur de risque d’OMD dans les études épidémiologiques ;
– le syndrome d’apnée du sommeil, observé chez près de la moitié des patients atteints d’OMD, a également été suggéré comme facteur d’entretien de l’OMD en raison de l’hypoxémie et des modifications métaboliques engendrées.
Par ailleurs, plus la RD est sévère, plus le risque d’OMD est important. La survenue d’un OMD durant la grossesse en est l’exemple. En effet, la grossesse est une période à haut risque d’évolution de la RD au cours de laquelle peut apparaître, lors de l’aggravation de l’atteinte rétinienne, un OMD. Disparaissant le plus souvent après l’accouchement, il n’est pas recommandé de le traiter pendant la grossesse. Dans tous les cas, les anti-VEGF doivent être évités, le VEGF jouant un rôle fondamental dans le développement du fœtus.
Enfin, la chirurgie de la cataracte peut favoriser l’apparition ou l’aggravation d’un OMD. Survenant en général 6 semaines après la chirurgie, il peut en altérer le bénéfice visuel et nécessiter le recours à des IVT. Au-delà de la réduction du risque infectieux, il est essentiel de contrôler de façon optimale en préopératoire la glycémie et la pression artérielle pour s’affranchir de ces facteurs de risque d’OMD.
Traitement de l’OMD
Objectif du traitement
Le traitement de l’OMD fait l’objet de recommandations en France(5). Plus qu’un gain d’AV sous traitement, la principale attente du patient est d’atteindre une AV lui permettant de reprendre ses activités quotidiennes qui étaient impactées par la baisse visuelle.
Néanmoins, la réponse thérapeutique peut être dissociée. Certains patients répondront sur le plan anatomique mais ne récupéreront pas une AV suffisante. En effet, la diminution de l’épaisseur maculaire évaluée par OCT ne prédit pas pour autant la réponse visuelle. Autant elle est un prérequis à l’amélioration de l’AV, autant elle n’est pas le seul déterminant de l’AV finale.
Moyens thérapeutiques
• Plusieurs traitements sont aujourd’hui disponibles pour traiter l’OMD. Outre le contrôle des facteurs systémiques indispensable dans tous les cas, des traitements ophtalmologiques s’avèrent aussi souvent nécessaires. Une photocoagulation au laser, des IVT ou dans certains cas une chirurgie oculaire peuvent alors être proposées.
• Leurs indications respectives sont aujourd’hui bien codifiées et celles du laser plus restreintes depuis l’avènement des IVT indiquées en première intention en cas d’OMD diffus avec baisse visuelle. Enfin, une vitrectomie sera discutée en cas d’OMD tractionnel.
Contrôler les facteurs systémiques : pierre angulaire du traitement
• Contrôle de l’équilibre glycémique
Dès les années 1990, de grandes études d’intervention (DCCT, UKPDS) ont démontré le bénéfice du contrôle glycémique sur l’évolution de la RD. Ces résultats ont été confirmés dans l’étude ACCORD Eye Study où le risque de progression de la RD était réduit de 33 % (p = 0,003) au terme de 4 ans de suivi chez les patients diabétiques de type 2 sous traitement intensif (HbA1c : 6,4 %) vs standard (HbA1c : 7,5 %)(6). Fait remarquable, cette diminution du risque de progression persistait plusieurs années après la fin de ces études chez les patients initialement inclus dans le groupe intensif et ce, en dépit d’un taux d’HbA1c convergent entre les 2 groupes(7).
Ces résultats ont donné lieu au concept de « mémoire glycémique ». Ils montrent aussi que normaliser secondairement les glycémies ne suffit pas à effacer les effets néfastes des années d’hyperglycémie, soulignant l’importance d’instituer, dès le diagnostic du diabète, un contrôle glycémique optimal conduisant à un taux d’HbA1c proche de 7 %.
Par ailleurs, aucun traitement hypoglycémiant n’a aujourd’hui montré sa supériorité pour freiner l’évolution de l’OMD. À l’inverse, de rares cas d’OMD ont été rapportés sous glitazones. Mais, dans l’étude ACCORD où les glitazones ont été largement prescrites dans le groupe intensif, l’incidence des événements microvasculaires était pourtant réduite comparée au groupe contrôle(6). Par ailleurs, dans une étude récente évaluant les facteurs prédictifs de réponse au traitement par IVT, le bénéfice visuel était similaire quel que soit le traitement hypoglycémiant (insuline, glitazones, etc.)(8). Enfin, l’augmentation des événements rétiniens, bien que rares, observée dans l’étude SUSTAIN-6(9) chez les patients diabétiques de type 2 inclus dans le groupe traité par semaglutide vs placebo fait l’objet de discussion. Une des hypothèses évoquées par les auteurs serait que ces complications rétiniennes soient la conséquence d’une baisse glycémique rapide chez des patients dont le taux d’HbA1c initial était élevé et atteints d’une RD à l’inclusion. En revanche, dans l’étude LEADER qui comparait le liraglutide à un placebo(9), le risque oculaire n’était pas augmenté chez les patients traités par liraglutide chez lesquels l’amplitude de baisse glycémique était moindre que dans l’étude SUSTAIN-6.
• Contrôle de l’équilibre tensionnel
Le bénéfice du contrôle tensionnel sur l’évolution de l’OMD a été démontré par plusieurs études d’intervention, dont l’UKPDS où la survenue d’une baisse visuelle était réduite de 47 % par diminution de l’incidence de l’OMD chez les patients inclus dans le groupe « contrôle tensionnel intensif » vs standard. Plus récemment, dans la sous-étude ADREM de l’essai randomisé ADVANCE, la survenue d’un OMD était réduite chez les patients traités par perindopril-indapamide vs placebo (OR 0,50 ; IC95% : 0,29-0,88). En revanche, dans l’étude ACCORD, aucune différence de progression de la RD n’était observée entre le groupe de patients diabétiques dont la pression artérielle (PA) systolique était < 120 vs 140 mmHg(6). Ces résultats suggèrent l’existence d’un effet seuil avec une absence de bénéfice supplémentaire pour des valeurs de PA plus basses. Ainsi, la PA cible conseillée est de 130/80 mmHg. Soulignons l’absence de « mémoire tensionnelle » imposant un contrôle tensionnel permanent, l’effet bénéfique s’estompant rapidement après l’arrêt du traitement antihypertenseur. Enfin, optimiser l’équilibre tensionnel permet aussi dans ce contexte d’éviter la survenue d’une rétinopathie hypertensive qui aggraverait le pronostic oculaire.
• Contrôle de la dyslipidémie
Deux larges études randomisées ont récemment suggéré l’intérêt d’un traitement par fénofibrate pour freiner l’évolution de la RD. Dans l’étude FIELD ayant inclus 9 795 patients diabétiques de type 2, ceux traités par fénofibrate 200 mg/j vs placebo nécessitaient plus rarement un traitement par laser (3,6 % vs 5,2 %, soit une réduction de 23 %)(10). Cet effet ne semblait pas lié à la diminution du taux de lipides, les taux de HDL-cholestérol et des triglycérides étant similaires chez les patients traités ou non par laser. Dans l’interprétation de ces résultats et leurs implications cliniques, il est important de signaler que l’évolution de la RD n’était pas le critère de jugement principal et les indications de laser non rapportés. Dans la seconde étude, l’étude ACCORD Eye Study incluant 2 856 patients diabétiques de type 2, la progression de la RD après 4 ans de suivi était réduite de 40 % chez les patients sous fénofibrate 160 mg/j + simvastatine vs simvastatine seule(6) mais ce bénéfice ne persistait pas à l’arrêt du fénofibrate(7). Des effets non lipidiques du fénofibrate pourraient rendre compte de son action bénéfique sur la RD. En effet, en tant qu’agoniste PPAR alpha, il réduit l’expression de VEGF et posséderait une action antioxydante et anti-inflammatoire bénéfique pour la rétine. Néanmoins, le niveau de preuve est aujourd’hui insuffisant pour proposer ce traitement en première intention chez des patients dyslipidémiques atteints de RD.
• Recherche et contrôle d’un syndrome d’apnée du sommeil (SAS)
Même si aucune étude randomisée n’a, à ce jour, démontré le bénéfice de la correction du SAS sur l’évolution de l’OMD, sa recherche et son contrôle sont recommandés. Une seule étude non randomisée incluant 32 patients a montré une meilleure AV à 6 mois chez les patients utilisant la CPAP > 2,5 vs < 2,5 h/nuit sans toutefois de bénéfice sur l’évolution de l’OMD. La durée de l’étude était certainement trop courte pour observer un effet positif et la compliance thérapeutique des patients trop souvent aléatoire.
Autres traitements évalués
Si les rôles de l’aldose réductase, de la protéine kinase C (PKC), des produits avancés de la glycation sont bien établis dans la pathogénie de l’OMD, aucune étude clinique réalisée avec leurs inhibiteurs respectifs, dont la ruboxistaurine, inhibiteur spécifique de l’isoforme β de la PKC, n’a montré de bénéfice significatif sur l’évolution de l’OMD.
Injections intravitréennes : traitement intensif et suivi rapproché pour une efficacité optimale
Les IVT constituent aujourd’hui le traitement de première intention en cas de baisse visuelle liée à un OMD sévère avec une atteinte centrale(5). Ces traitements, au-delà de leur coût, imposent au patient des injections répétées et un suivi ophtalmologique rapproché. Deux classes thérapeutiques sont aujourd’hui disponibles : les anti-VEGF et les corticoïdes.
• Les anti-VEGF
Le ranibizumab (Lucentis®, Novartis) a été, en 2012, la première molécule anti-VEGF à obtenir l’AMM pour le traitement de l’OMD atteignant la région centrale et associée à une baisse significative de l’AV. Son efficacité vs placebo et sa supériorité vs laser ont été démontrées dans plusieurs études randomisées (RESTORE, DRCRnet, RISE and RIDE). En moyenne, le gain d’AV au terme de 2 ans de traitement était de 2 à 3 lignes (10 à 15 lettres) au prix d’un nombre moyen d’injections compris entre 7 et 9 la première année et 4-5 la deuxième année.
Ces études nous ont aussi appris que le traitement devait être débuté sans trop tarder, le bénéfice oculaire étant meilleur lorsque la durée de l’OMD est plus courte et l’AV initiale moins faible(11). En effet, plus l’œdème est ancien, plus la fonctionnalité des cellules rétiniennes est altérée et les capacités de récupération visuelle amoindries. Ce traitement a aussi montré son efficacité à ralentir la progression de la RD chez les patients traités par anti-VEGF pour un OMD.
Plus récemment, l’aflibercept, un VEGF-Trap-eye (Eylea®, Bayer), dont l’efficacité a été démontrée par les études VIVID et VISTA(12), a obtenu une AMM pour le traitement de l’OMD avec une indication similaire à celle du ranibizumab mais des modalités de traitement et de fréquence d’injections différentes.
Le choix entre ces deux anti-VEGF est laissé à la libre appréciation des ophtalmologistes, aucune donnée ne les ayant comparés face à face aux doses commercialisées en France, soit 0,5 mg pour ranibizumab et 2 mg pour aflibercept. La seule étude publiée, le protocole T dont les résultats sont résumés ci-dessous, comparait ces deux molécules mais à des doses différentes de celles recommandées en France, notamment plus faible (0,3 mg) pour ranibizumab.
Protocole T(13)
Le DRCR.net (Diabetic Retinopathy Clinical Research Network) est un réseau collaboratif regroupant 115 sites et plus de 400 praticiens aux États-Unis. Il est à l’initiative de nombreux essais cliniques évaluant l’efficacité et la tolérance des IVT dans l’OMD, dont le protocole T comparant l’efficacité à 2 ans de 3 anti-VEGF, le ranibizumab 0,3 mg (dose plus faible que celle commercialisée en France), l’aflibercept 2 mg et le bevacizumab 1,25 mg. Les patients ont reçu une dizaine d’injections en moyenne la première année et une quinzaine au total en 2 ans, soit une réduction de 40 % la deuxième année. Deux tiers des patients (64 %) inclus dans le groupe bevacizumab ont bénéficié d’un traitement complémentaire par laser, la moitié (52 %) de ceux du groupe ranibizumab et 41 % de ceux du groupe aflibercept. L’efficacité clinique était globalement équivalente pour les trois traitements à l’exception de l’aflibercept plus efficace à un an que ranibizumab 0,3 mg ou bevacizumab en cas d’AV initiale basse (≤ 4/10e). Mais cette différence d’efficacité s’estompait après 2 ans de suivi. Enfin, le taux d’événements cardiovasculaires à 2 ans variait entre les trois molécules (8 % sous bevacizumab, 12 % ranibizumab et 5 % aflibercept ; p = 0,047), mais cette différence n’a pas été retrouvée dans les autres études.
Le schéma thérapeutique selon l’AMM débute par une phase d’induction à raison d’une injection mensuelle pendant 3 mois consécutifs pour ranibizumab et 5 mois pour aflibercept. Elle permet d’évaluer la réponse anatomique (épaisseur maculaire évaluée par OCT) et fonctionnelle (AV) au traitement. Les IVT sont ensuite poursuivies chez les patients « répondeurs » à un rythme rapproché jusqu’à stabilisation de l’AV et de l’épaisseur maculaire. La troisième phase permet d’éviter la récidive de l’OMD. Le traitement y est administré à une fréquence déterminée par l’évolution des paramètres oculaires. En revanche, en l’absence de bénéfice, le traitement par anti-VEGF est interrompu et une autre classe thérapeutique (corticoïdes) proposée en l’absence de contre-indication.
Enfin, la tolérance systémique a été jugée globalement bonne dans les essais cliniques. Rares sont les patients inclus ayant présenté des événements cardiovasculaires (CV) mais ceux avec des antécédents CV récents étaient exclus. Or, la survenue d’accidents CV, rapportés chez des patients traités par anti-VEGF par voie systémique en oncologie, demeure un risque potentiel chez un patient traité par IVT d’anti-VEGF et en dépit du faible passage systémique après IVT. Ainsi, la prudence recommande de ne pas injecter d’anti-VEGF dans les 3 mois suivant un accident vasculaire cérébral (AVC) ou un infarctus du myocarde (IDM), d’autant plus que le risque CV est déjà majoré en cas d’OMD(14).
• Les corticoïdes
Compte tenu du rôle de l’inflammation dans la pathogénie de l’OMD, l’utilisation de corticoïdes représente une alternative thérapeutique intéressante. Leur administration par voie intravitréenne permet de s’affranchir du risque de décompensation du diabète en raison du très faible passage systémique après IVT. En outre, leur durée d’action, plus longue que celle des molécules anti-VEGF, permet de réduire la fréquence des injections. En revanche, leurs effets secondaires, au premier rang desquels le risque de cataracte et d’augmentation de la pression intraoculaire, doivent être soulignés et conditionnent le choix thérapeutique.
Deux traitements à base de corticoïdes ont récemment obtenu l’AMM dans cette indication. La triamcinolone, utilisée avec une certaine efficacité pendant plusieurs années mais sans AMM pour une utilisation intravitréenne, n’est plus employée aujourd’hui en France au profit des produits ayant obtenu l’AMM dans l’OMD.
Le premier traitement est un implant biodégradable à libération progressive contenant 700 μg de dexaméthasone (Ozurdex®, Allergan). Son efficacité a été démontrée dans l’étude MEAD(15) et sa durée d’action de l’ordre de 3 à 4 mois. Ce traitement est indiqué en première intention chez les patients ayant des contre-indications au traitement par anti-VEGF, ceux ayant présenté récemment un AVC ou un IDM ou ne pouvant pas se déplacer souvent. Il est recommandé chez des patients déjà opérés de cataracte (pseudophakes) en raison du risque induit d’opacification du cristallin. En revanche, il est contre-indiqué en cas de glaucome évolué ou non équilibré. Il est aussi proposé en deuxième intention chez les patients dont la réponse thérapeutique aux anti-VEGF est insuffisante.
Le deuxième traitement est un implant non biodégradable d’acétonide de fluocinolone (Iluvien®, Alimera) à longue durée d’action, dont l’efficacité a été démontrée dans l’étude FAME(16). Son effet thérapeutique serait de 2 à 3 ans. Il pourra être proposé aux patients non répondeurs aux anti-VEGF après s’être assuré que les corticoïdes intravitréens de courte durée d’action ont été efficaces et bien tolérés sans hypertonie oculaire sévère.
Schéma thérapeutique de l’OMD
Le choix du traitement est guidé par l’analyse du bilan préthérapeutique détaillé dans la figure 4.
Figure 4. Bilan préthérapeutique.
En l’absence de baisse visuelle et au-delà de la surveillance préconisée, le seul traitement recommandé est le laser. Indiqué en cas d’OMD modéré ou sévère lorsque les microanévrysmes sont accessibles au laser, il sera débuté rapidement en cas de menace visuelle.
En cas de baisse visuelle liée à un OMD sévère avec une atteinte centrale, les IVT constituent le traitement de première intention. Plusieurs études se sont intéressées aux facteurs permettant d’identifier le profil du patient « répondeur » au traitement et de se prononcer sur sa probabilité de récupération visuelle. Ainsi, une longue durée d’évolution de l’OMD, une AV initiale basse, une faible compliance thérapeutique associée à un contrôle suboptimal des facteurs de risque systémiques ou une ischémie maculaire sont associés à un mauvais pronostic oculaire ou une moindre réponse au traitement par IVT.
Conclusion
Même si le pronostic visuel des patients atteints d’OMD a été largement amélioré depuis l’avènement des injections intra-oculaires, ces traitements sont coûteux et leur réponse variable d’un patient à l’autre.
En outre, au-delà de l’équilibre indispensable des facteurs systémiques pour traiter l’OMD, les études nous ont appris la nécessité d’une prise en charge intensive pour une efficacité optimale.
Ces constats justifient de mieux définir les facteurs prédictifs de réponse au traitement dans un contexte économique contraint. Le résultat des prochaines études nous donnera probablement des indications pour y répondre.
En perspective, la meilleure compréhension des mécanismes impliqués dans la pathogénie de l’OMD contribuera au développement de stratégies thérapeutiques émergentes, dont certaines sont déjà en cours d’évaluation.
Figure 5. Schéma thérapeutique en cas d’OMD.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :