Publié le 15 juin 2018Lecture 8 min
Une goutte et des lithiases urinaires bien précoces !
Claire DOUILLARD, Service d’endocrinologie-diabétologie-métabolisme, Hôpital Huriez, CHRU de Lille, Centre de référence des maladies héréditaires du métabolisme, Lille
L’hyperuricémie liée à une erreur innée du métabolisme est rare et parfois de diagnostic difficile à l’âge adulte. Nous rapportons ici le cas d’un patient chez qui le diagnostic a été posé vers l’âge de 50 ans, l’hypothèse ayant été suggérée du fait de la survenue précoce de coliques néphrétiques et d’épisodes de goutte.
Observation
Le patient est un homme de 50 ans qui a été admis en réanimation pour prise en charge d’un choc septique sur une cellulite de la jambe droite ayant évolué vers une défaillance multiviscérale, dont une insuffisance rénale aiguë oligo-anurique.
La porte d’entrée de cet épisode septique était une petite plaie du pied droit évoluant vers une fascéite nécrosante chez un patient traité par AINS depuis environ une semaine pour soulager une colique néphrétique. Après prise en charge chirurgicale (nécrosectomie) et médicale ayant nécessité 2 séances d’hémodialyse, la fonction rénale s’était complètement normalisée (créatine 11 mg/l [97 μmol/l]), mais le patient a présenté un peu plus de 6 semaines après sa première admission un 2e épisode d’insuffisance rénale aiguë obstructive (créatinine à 20 mg/l [177 μmol/l]) secondaire à une cristallisation massive des deux uretères en moins de 2 mois.
À ce stade, la reprise de l’interrogatoire a permis de collecter des données anamnestiques manifestes. Si les antécédents familiaux sont pauvres au sein de cette fratrie de 5 enfants, sans problème particulier (sous réserve d’une enquête limitée par rupture familiale), les antécédents personnels sont en revanche riches : le patient décrit des crises d’arthrite aiguë depuis l’âge de 16 ans ayant commencé au niveau des articulations métatarso-phalangiennes puis s’étendant aux genoux, aux coudes et aux poignets. Ces épisodes survenaient au moins une fois/mois avec une consommation importante de colchicine. La nature microcristalline de ces arthrites a été confirmée à l’âge de 45 ans lors de l’examen du liquide de ponction articulaire (microcristaux d’urate de sodium et de pyrophosphate de calcium). Les crises se sont espacées avec la prescription d’allopurinol à l’âge de 46 ans. La maladie lithiasique urinaire a commencé à 18 ans avec 3 épisodes de coliques néphrétiques par an, de façon bilatérale, plus fréquemment à droite. Le scanner des voies urinaires montrait il y a 4 ans de nombreux calculs bilatéraux prédominant sur le rein gauche avec une taille maximale de 8 mm et surtout d’une densité élevée à 371 UH. L’uricémie était à l’époque à 160 mg/l (30-70) puis recontrôlée à 74 mg/l après mise sous allopurinol 100 mg/j suivi d’un quasi-amendement des épisodes de coliques néphrétiques (un seul épisode en 4 ans). Enfin, l’autre antécédent majeur de ce patient est un infarctus du myocarde ayant nécessité la pose d’un stent sur la diagonale il y a 4 ans. Cet épisode s’inscrivait dans un contexte de surcharge pondérale (100 kg pour une taille de 1,72 m, soit un IMC à 33,8) et un tabagisme (risque estimé à 30 PA).
L’examen clinique lors de ces hospitalisations ne relevait pas de tophi, ni de point d’appel neurologique, en particulier pas de dystonie, ni de syndrome pyramidal ou extrapyramidal, ni de trouble du comportement. Le patient rapporte toutefois des difficultés scolaires avec un parcours chaotique, sans diplôme ni qualification. Il est employé en boulangerie. Sa fille unique est en bonne santé.
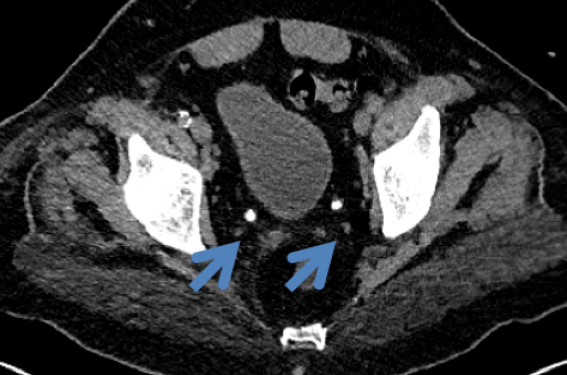
Ce 2e épisode d’insuffisance rénale aiguë a été rattaché à une cristallisation massive des deux uretères. Lors de sa première admission, l’acide urique en réanimation avait atteint 263 mg/l (30-70) et se maintenait > 120 mg/l malgré la normalisation de la fonction rénale. Le pH urinaire était à 5,2. La densité des cristaux était de 307 UH sur le scanner (figure 1).
Figure 1. TDM rénal et des voies excrétrices urinaires : cristallisation des cavités excrétrices et des uretères. A : à gauche ; B : à droite ; C : au niveau des 2 uretères (lithogenèse intense, bilatérale, d’installation rapide en moins de 2 mois).
Une dérivation des urines a été réalisée en urgence. Il n’y a pas eu d’analyse spectrophotométrique des lithiases, mais la cristallurie sur les urines fraiches a confirmé la présence de nombreux cristaux d’urates amorphes complexes, ainsi que quelques cristaux d’acide urique dihydraté. En regard d’une créatinine à 24 mg/l, on relevait un acide urique sérique à 92 mg/l et sur un volume de 3 000 ml/24 h, les caractéristiques métaboliques étaient les suivantes :
– pH 5,7
– Na : 273 mmol/24 h (14 g/24 h)
– calciurie 11 mg/l (0,28 μmol/l) et 33 mg/24 h (0,84 μmol/24 h)
– phosphaturie : 65 mg/l (2,08 mmol/l) et 195 mg/24 h (6,24 mmol/24 h)
– uricurie 632 mg/L (3,5 mmol/l) et 1 897 mg/24 h(10,5 mmol/24 h) (N : 300-750 mg/24 h)
– créatinine 1 029 mg/24 h (9 107 μmol/24 h).
La prise en charge néphrologique a consisté à procéder à une alcalinisation des urines par perfusion de bicarbonates de sodium en intraveineux adaptés au pH urinaire ainsi qu’à la reprise du traitement par allopurinol. L’évolution a été favorable sur le plan rénal avec une récupération complète des valeurs de créatinine à 12 mg/l. Le pH urinaire restait entre 6 et 7,2. Les perfusions ont pu être relayées par du bicarbonate per os sous forme d’1 l d’eau de Vichy.
Le scanner rénal de contrôle 3 semaines après a montré une fonte complète des lithiases (figure 2B), autorisant l’ablation des sondes JJ.
Figure 2. TDM rénal et des voies excrétrices urinaires (après reconstruction). A : avant traitement ; B : 3 semaines après traitement (alcalinisation, allopurinol) : fonte des lithiases.
Plusieurs hypothèses expliquant cette cristallisation massive d’acide urique dans les cavités excrétrices pouvaient à ce stade être formulées :
– anomalie congénitale de métabolisme des purines prédisposant à l’hyperuricémie ;
– arrêt de l’allopurinol lors du passage initial en réanimation et défaut d’élimination urinaire de l’acide urique (premier épisode d’insuffisance rénale) responsables d’une hyperuricémie majeure ;
– puis, récupération de la fonction rénale avec reprise de diurèse, conduisant à une charge filtrée majeure en acide urique avec hyperuricurie, en urine acide (favorisant la cristallisation).
L’hypothèse d’une erreur innée du métabolisme et notamment d’un déficit de l’activité en hypoxanthine phosphoribosyltransférase (HPRT) a été explorée. Cette enzyme constitue une étape clé du métabolisme de l’acide urique puisque l’HPRT permet de limiter la synthèse de l’acide urique en constituant une voie dite « de sauvetage », qui reconvertit les bases puriques hypoxanthine et guanine vers l’élaboration de leurs nucléotides respectives, participant ainsi au renouvellement des acides nucléiques (figure 3).
Figure 3. Métabolisme simplifié de l’acide urique, non exhaustif de l’ensemble des étapes enzymatiques impliquées.
Un dosage de l’activité HPRT sur érythrocytes a été réalisé par méthode radio-enzymatique (Dr I. Ceballos-Picot, laboratoire de biochimie métabolomique et protéomique, Hôpital Necker). L’activité de l’enzyme HPRT a été retrouvée basse à deux reprises : 0,7 nmol/min/mg Hb (2-2,9). Le déficit en HPRT a été confirmé sur le plan génétique lors de l’analyse par PCR-séquençage du gène HPRT (Xq26-27.2) mettant en évidence une mutation hémizygote c.166G>A.
Par la suite, le traitement par allopurinol a été augmenté progressivement par titration en fonction de la surveillance notamment de la xanthinurie et l’hypoxanthinurie par chromatographie urinaire (à risque d’élévation du fait de l’inhibition de la xanthine oxydase (figure 3), ce qui favoriserait la survenue de cristaux et calculs de xanthine). La titration optimale de la posologie d’allopurinol sera finalement de 300 mg/j : créatinine 11 mg/l, acide urique 95 mg/l, uricurie (1 405 mg/24 h), EF(acU) 0,09 % versus 0,48 % (avant traitement). En sus de l’allopurinol et la diurèse alcaline et au vu du contexte métabolique, des conseils ont été donnés pour limiter de principe les aliments très riches en purines (abats, bouillon de viande, sardines, anchois, harengs, alcool) et ceux riches en purines (viandes, volailles, poissons, crustacés, pois, haricots, lentilles), tout en couvrant les besoins protidiques.
Discussion
L’hyperuricémie est définie par la concentration sérique au-dessus de laquelle il existe un risque de manifestations cliniques (accès de goutte articulaire, lithiases urinaires, insuffisance rénale).
Quand il existe une hyperuricémie, le plasma et les liquides extracellulaires sont saturés, en particulier en urates, d’où la formation de cristaux et de dépôts tissulaires. Plusieurs erreurs innées du métabolisme de l’acide urique ont été décrites et identifiées en fonction de l’étape enzymatique déficitaire. Le déficit en HPRT(1) est l’une d’entre elles et est une cause grave d’hyperuricémie héréditaire. Il s’agit d’une maladie récessive liée à l’X du fait d’une mutation du gène HPRT1. La profondeur du déficit de l’activité enzymatique est variable en fonction du type de mutation et conditionne le phénotype. Il existe plus de 600 mutations décrites. Le déficit complet correspond à la maladie de Lesch-Nyhan(2) (prévalence 1/380 000 à 1/235 000) caractérisée chez le garçon par des lithiases urinaires avec néphropathie urique, une goutte gravissime, des troubles neurologiques (hypertonie, syndrome extrapyramidal, mouvements athétosiques) et neuropsychiatriques (troubles du comportement avec automutilation). Il y a également des formes atténuées de la maladie (patients « Lesch-Nyhan variants »)(3), dont les symptômes sont mineurs ou absents ou se manifestant par des complications liées à l’hyperuricémie (patients « HRH » ou « HPRTrelated hyperuricemia »)(4) mais sans troubles neurologiques. Le cas du patient que nous avons rapporté ici s’inscrit dans ce cadre. Enfin, parmi ces formes atténuées, certains patients peuvent présenter des troubles neurologiques mais sans trouble du comportement (HPRT-related neurological dysfunction).
Concernant le traitement, l’allopurinol, inhibiteur de la xanthine oxydase, présente une analogie structurale avec l’hypoxanthine (substrat de l’HPRT), ce qui explique qu’il peut à forte dose être un inhibiteur de l’HPRT. De ce fait, en cas de déficit partiel de l’HPRT, il est souhaitable d’utiliser le febuxostat qui est un inhibiteur spécifique de la xanthine oxydase, sans impact sur l’HPRT, ce qui évite de supprimer l’activité enzymatique résiduelle. Enfin, en cas de traitement par allopurinol, un suivi de la cristallurie (recherche des cristaux de xanthine en particulier) est nécessaire, comme cela a été proposé chez ce patient, car le double déficit (HPRT + xanthine oxydase par le traitement allopurinol) entraine la formation de cristaux et de calculs de xanthine si le traitement en allopurinol est surdosé.
Conclusion
Des manifestations précoces d’hyperuricémie (goutte, lithiases urinaires à répétition), notamment avant 25 ans, suggèrent une anomalie héréditaire du métabolisme de l’acide urique.
Celle-ci peut être confirmée sur le plan enzymatique et génétique s’il s’agit par exemple d’un déficit en HPRT lié à l’X.
L’enjeu diagnostique est important pour éviter notamment les destructions ostéoarticulaires liées à la gravité de ces formes de goutte et un retentissement rénal parfois dramatique.
La posologie du traitement doit être ajustée en fonction de son efficacité et sa tolérance.
Enfin, une information et un dépistage familial sont à proposer au cours d’une consultation en génétique médicale.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :




