Publié le 28 fév 2011Lecture 9 min
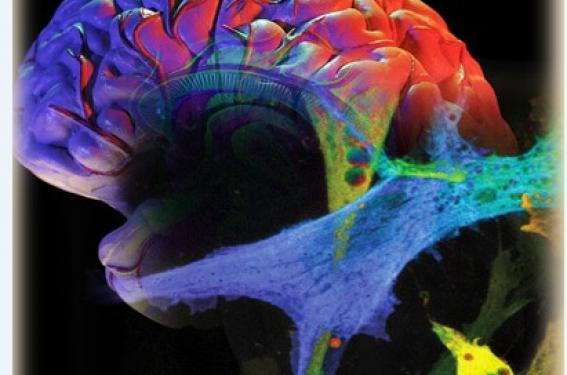
Cerveau et diabète
M. DEKER
Journée thématique organisée par la Société francophone du diabète
Nouvelles données concernant le métabolisme énergétique cérébral
D’après la communication de L. Pellerin (Lausanne)
Bien que le cerveau représente environ 2 % du poids corporel, il reçoit près de 15 % de l’apport sanguin et consomme au moins 25 % du glucose et 20 % de l’oxygène. Le métabolisme oxydatif du glucose représente donc une voie majeure de la production énergétique cérébrale.
Quatre points résument les notions consensuelles concernant le métabolisme énergétique cérébral :
• le glucose est le substrat énergétique principal utilisé par le cerveau adulte, avec des exceptions toutefois puisque les corps cétoniques représentent un substrat d’appoint chez le nourrisson ; lorsque les concentrations de lactates sont suffisantes (par exemple, lors d’un exercice physique), ces derniers peuvent remplacer le glucose au niveau cérébral ;
• l’oxydation du glucose fournit toute l’énergie nécessaire pour le cerveau ;
• l’activité neuronale consomme 80 à 95 % de la dépense énergétique cérébrale totale alors que la glie n’en consomme que 5 à 20 % ;
• il existe une relation étroite entre activité cérébrale, débit sanguin et consommation de glucose.
Le lien entre activité cérébrale, débit sanguin et consommation de glucose a longtemps été expliqué au moyen d’un schéma simple : en réponse à une augmentation de l’activité neuronale, certains mécanismes permettraient de libérer des substances vasodilatatrices, lesquelles augmenteraient le débit sanguin local, ce qui fournirait les substrats nécessaires aux neurones qui en ont besoin.
Les astrocytes, un rouage essentiel
Ce modèle est toutefois remis en question aujourd’hui par la reconnaissance du rôle joué par les astrocytes. Le système nerveux central n’est pas seulement composé de neurones et de vaisseaux sanguins ; entre eux figure toujours au moins un processus astrocytaire. Des processus astrocytaires, comportant des récepteurs pour la plupart des neurotransporteurs, entourent les synapses neuronales, ce qui suggère que ces cellules pourraient détecter l’activité synaptique ; d’autres processus astrocytaires, comportant des récepteurs des transporteurs du glucose, entourent les vaisseaux sanguins. D’où l’idée que les astrocytes pourraient jouer un rôle de couplage entre l’activité neuronale et l’approvisionnement en glucose. Pour que ce modèle fonctionne il faut que le glucose capté par les astrocytes soit libéré par ces derniers en fonction des besoins des neurones.
Une étude récente apporte des arguments en faveur de cette hypothèse(1) en montrant une accumulation préférentielle d’un analogue fluorescent du glucose dans les astrocytes après stimulation corticale chez le rat.
Le lactate, un substrat additionnel
L. Pellerin et coll. ont élaboré un modèle permettant d’expliquer le mécanisme du couplage entre l’activité neuronale et la consommation de glucose, qui fait intervenir le recyclage du glutamate en lactates par les astrocytes, le lactate étant un substrat énergétique additionnel libéré dans l’espace intercellulaire(2). La présence dans les espaces intercellulaires de glucose et de lactate en concentrations équivalentes, pose la question de l’utilisation préférentielle de l’une de ces substances par les neurones. Plus la concentration de lactate augmente, plus il semble que ce dernier soit le substrat préférentiel du processus oxydatif ; en conditions proches des conditions physiologiques, le lactate fournit les trois quarts de l’apport énergétique des neurones.
Ces travaux récents ont abouti à renouveler les concepts en matière de physiologie énergétique cérébrale. Après activation neuronale, le glucose est capté par les astrocytes qui vont le convertir en lactate et le libérer dans l’espace extracellulaire au moyen d’un transporteur spécifique. Les neurones, qui possèdent aussi un transporteur de lactate, le captent du milieu extracellulaire pour le retransformer en glucose. Si le glucose demeure un substrat énergétique important pour les neurones, son métabolisme est donc plus complexe qu’on ne l’imaginait et, dans certaines circonstances, d’autres métabolites intermédiaires comme les lactates, prennent une place préférentielle par rapport au glucose.
Références
1. Chuquet J et al. J Neurosci 2010 ; 30 : 15298-303.
2. Jolivet R et al. J Cereb Blood Flow Metab 2010 ; 30 : 1982-6.
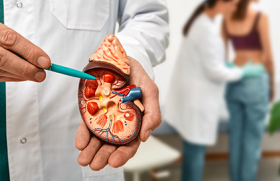
Les hypoglycémies chez le diabétique
D’après la communication d’A. Graveling (Edinburgh)
Les hypoglycémies asymptomatiques sont beaucoup plus fréquentes que les hypoglycémies symptomatiques chez le diabétique. En pratique, on distingue deux types d’hypoglycémies, selon qu’elles sont modérées permettant le resucrage, ou sévères nécessitant l’assistance d’un tiers. La définition biochimique des hypoglycémies est variable, allant de < 2,1 mmol/l (0,37 g/l) à < 3,9 mmol/l (0,7 g/l).
Une symptomatologie variable et évolutive
Chez le diabétique de type 1, on estime à 2 épisodes hebdomadaires la fréquence des hypoglycémies modérées. Un tiers des patients présentent une hypoglycémie sévère par an. Chez le diabétique de type 2, la prévalence des hypoglycémies sévères est d’environ 7 % chez les patients traités par sulfamides hypoglycémiants, équivalente à celle des hypoglycémies chez les patients sous insuline depuis moins de 2 ans.
La symptomatologie des hypoglycémies est variable selon les individus et elle évolue avec le temps. Les symptômes les plus fréquents sont les sueurs et les tremblements, surtout chez les sujets jeunes, alors que les sujets âgés présentent majoritairement des symptômes neurologiques (ataxie, troubles visuels). Plus d’un tiers des hypoglycémies sévères survenant en période de veille peuvent ne pas s’accompagner de symptôme d’alerte et de nombreux diabétiques traités par insuline perdent leur capacité à identifier le début de la crise, syndrome identifié comme une altération de la perception des hypoglycémies, qui est considéré comme une complication du traitement insulinique et serait responsable d’hypoglycémies sévères.
Facteurs de risque des hypoglycémies sévères chez le diabétique
- Ancienneté du diabète
- Ancienneté du traitement insulinique
- Contrôle glycémique strict
- Antécédents d’hypo-glycémies sévères
- Survenue pendant le sommeil
- Insuffisance rénale
- Altération de la perception des hypoglycémies
Le syndrome d’altération de la perception des hypoglycémies
L’altération de la perception des hypoglycémies est due à une défaillance du système nerveux autonome entraînant une diminution de la réponse adrénergique à l’hypoglycémie aiguë, alors même que le système de contre-régulation par le glucagon décline rapidement sous traitement insulinique, pour disparaître au bout de 5 ans. Progressivement, le seuil de stimulation du système autonome diminue jusqu’à des valeurs glycémiques critiques, d’où la disparition des symptômes d’alerte. Il semble néanmoins que ce soit la répétition des épisodes d’hypoglycémie qui soit responsable du développement de ce syndrome et non une atteinte primitive du système nerveux autonome.
Les approches thérapeutiques de ce syndrome impliquent une autosurveillance glycémique étroite et la révision des cibles glycémiques à la hausse, afin d’éviter au maximum les baisses dangereuses de la glycémie. Les analogues de l’insuline de longue durée d’action seraient associés à une moindre fréquence des hypoglycémies symptomatiques, nocturnes et non sévères. Il a également été montré que les bêta-agonistes diminuent le risque de survenue des hypoglycémies nocturnes, mais que ce bénéfice est compensé par une augmentation des hyperglycémies matinales. Par ailleurs, la caféine potentialise l’intensité des symptômes et améliore les réponses de contre-régulation.
Quelles sont les conséquences des hypoglycémies aiguës ?
D’après la communication de S. Halimi (Grenoble)
L’actualité récente, avec les résultats de l’étude ACCORD, a soulevé l’hypothèse d’un lien de causalité entre hypoglycémies et risque cardiovasculaire, qui expliquerait le surcroît de mortalité dans le groupe de traitement intensif. Se pose également la question des conséquences cérébrales des hypoglycémies, les syndromes déficitaires étant relativement exceptionnels.
De probables troubles du rythme
La responsabilité directe des hypoglycémies dans l’augmentation du risque de mortalité chez les patients bénéficiant d’un traitement intensif n’est pas parfaitement établie, même s’il a été montré que la survenue de plus de 3 hypoglycémies est associée à une augmentation de la mortalité. L’absence de lien de temporalité entre la survenue des hypoglycémies et les décès plaiderait contre cette hypothèse. En revanche, il est possible que la répétition des hypoglycémies constitue une sorte de préconditionnement au niveau myocardique et cérébral. Les auteurs de l’étude ACCORD récusent également un lien entre hypoglycémies, neuropathie autonome et mortalité.
En revanche, il a été montré que les hypoglycémies s’accompagnent d’anomalies électriques cardiaques (arythmies et troubles de la conduction) qui pourraient expliquer la survenue de décès subits pendant le sommeil et plus particulièrement ceux des jeunes diabétiques de type 1 victimes du syndrome « dead in bed » ; ces troubles rythmiques surviendraient après un certain délai faisant suite à l’hypoglycémie. Une autre explication serait le déclenchement par l’hypoglycémie de mécanismes inflammatoires procoagulants.
De rares séquelles cérébrales
Les conséquences cérébrales des hypoglycémies aiguës dépendent de la profondeur de l’hypoglycémie. Elles sont assez difficiles à évaluer car les épisodes d’hypoglycémie sont largement sous-estimés par les patients eux-mêmes. Une altération progressive des capacités cognitives, avec des troubles de l’adaptation et de l’humeur et parfois des crises comitiales, peut laisser la place à une altération de la conscience et à l’extrême à un coma avec comitialité et éventuellement séquelles, puis aboutir à un décès neuronal. Toutefois, la comitialité n’est pas contemporaine du nadir de la glycémie, mais la crise survient plusieurs heures après que la glycémie s’est abaissée, d’où l’intérêt des systèmes d’alarme chez les patients équipés d’un système de monitoring de la glycémie.
Dans la plupart des cas, les troubles cérébraux sont réversibles. La question des séquelles immédiates se pose essentiellement pour des situations rares, mais l’installation d’une démence consécutive à un épisode d’hypoglycémie sévère n’est pas démontrée. Les formes séquellaires les plus sévères sont surtout des lésions déficitaires qui surviennent pour un niveau de glycémie aux alentours de 0,18 g/l pendant une durée supérieure à 6 heures.
Tous les territoires cérébraux ne sont pas affectés de la même façon par l’hypoglycémie. Les lésions neuronales ne seraient pas dues à l’hypoglycémie elle-même mais à la libération massive de pyruvate et glutamate dans les espaces extracellulaires, qui agissent comme des toxines ; ce phénomène lésionnel aboutit à la libération de calcium et à la mort cellulaire. Cependant, grâce à des phénomènes de relais, le cerveau resterait longtemps alimenté du point de vue énergétique malgré la baisse de la glycémie et tolérerait davantage la baisse des ressources en glucose qu’il ne tolère l’hypoxie. Par ailleurs, la récupération des ressources énergétiques cérébrales interviendrait plus rapidement et la mort cellulaire plus tardivement chez les sujets ayant des antécédents d’hypoglycémies à répétition, ce qui alimente l’hypothèse d’un préconditionnement cérébral.
Chez le diabétique de type 2, ce sont les troubles cognitifs qui aggravent le risque d’hypoglycémie et non l’inverse. Plus le DT2 est anciennement insulinotraité, plus il est carencé en insuline, et plus son risque hypoglycémique est important. Chez ces patients, il faudrait probablement réviser les objectifs d’HbA1c à 7,5 %.
De même, il faut être prudent dans la conduite du contrôle glycémique chez les jeunes diabétiques de type 1 vivant seuls, cette condition étant associée à un surcroît de mortalité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :